2019年12 月,太阳集团tyc9728邓军教授课题组在《The Journal of Organic Chemistry》发表了题为“Enantioselective Syntheses of 4H�3,1-Benzoxazines via Catalytic Asymmetric Chlorocyclization of o�Vinylanilides”的研究论文。
4H-3,1-苯并恶嗪因其广泛的生物活性而在药物化学中是重要的杂环化合物具有重要的生物活性,如作为有价值的药物或生物活性试剂,在临床上已用于抗焦虑和抗惊厥,也被用作抗真菌剂和孕激素受体激动剂,因此对于其的合成在有机合成和医药领域引起科学家们的广泛关注。尽管科学家们已投入大量精力来合成苯并恶嗪衍生物,但对映选择性合成4H-3,1-苯并恶嗪的方法却仍旧很少。受前人研究以及不对称氯环化反应成功合成手性恶唑啉-二氢恶嗪和相关化合物的启发,太阳成集团邓军教授课题组找到了一种通过DCDMH为溴源通过邻乙烯基苯胺的氯环化合成新型手性4H-3,1-苯并恶嗪的方法。
该课题选择了易于合成的N-(2-(1-(苯基乙烯基)苯基)苯甲酰胺作为模型底物评估手性有机催化剂,对反应条件——催化剂、温度、溶剂、不同结构的卤源进行了优化,最终确定了以化合物VI(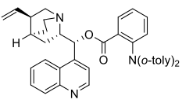 )为催化剂,MeOH作溶剂,-78 °C为反应温度,DCDMH(
)为催化剂,MeOH作溶剂,-78 °C为反应温度,DCDMH(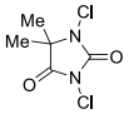 )作为氯源的最优条件。
)作为氯源的最优条件。
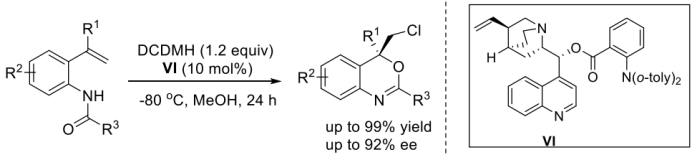
而后,他们为了考察该方法的适用性,对多个不同取代基底物进行了筛选,其中他们考察了一系列邻乙烯苯甲酰胺类底物以及酰胺部分具有不同取代基的底物,这些底物都显示出良好的收率以及ee值,表明该方法的适用性良好。
最后他们还提出了一种可能的催化模型。一方面,辛可尼丁部分的叔胺可能络合氯鎓离子,从而提供手性环境;另一方面,底物中的苯甲酰胺中的NH与MeOH介导的催化剂形成氢键,从而增加酰胺基团的亲核性。同时,上述两种作用形成的空间构象可能是控制对映选择性的因素。
该工作得到国家自然科学基金、太阳成集团等资助。
论文链接:https://pubs.acs.org/doi/pdf/10.1021/acs.joc.9b02395
责任编辑:肖文英